193. La densità delle miscele nelle immersioni
| In questo articolo prosegue il discorso su “Fisiologia respiratoria dell'immersione profonda - Seminario di Simon Mitchell”, pubblicato da "Teoria Subacquea" (https://m.facebook.com/story.php?story_fbid=140131864541995&id=110097917545390). |
|
Questa volta ci concentriamo sulla densità dei gas in immersione e su come questo parametro si modifichi al variare di profondità e miscela respirata. Partiamo dal paper di riferimento: “Respiratory Physiology of Rebreather Diving” (2015, Gavin Anthony e Simon J. Mitchell). All’interno della trattazione si trova un paragrafo intitolato “Consideration of gas density in diving planning”, nel quale in poche righe viene approfondito un concetto forse sottovalutato nella pianificazione delle immersioni. In sintesi: una società, la QinetiQ, ha generato un database di circa 450 immersioni completamente monitorate a differenti profondità e con diverse densità dei gas, con un protocollo di esercizi fino ad un lavoro pari a 125 W. Ha combinato tre fattori: profondità, densità e sforzo fisico. In particolare, l’immersione viene considerata fallita se lo sforzo respiratorio (ET CO2 – End Tidal CO2) supera gli 8,5 kPa (circa 64mm HG): “'dive failure' including: (any of) equipment or monitoring failure, diver unable or unwilling to continue because of dyspnoea (shortness of breath) or exhaustion, and an end-tidal CO2 >8.5 kPa (64 mm Hg) over five consecutive breaths.” I risultati sono raggruppati in un grafico a barre che ci mostra come il tasso di fallimento delle immersioni cresca al crescere della densità del gas misurata in g/L (grammi per litro). Mentre
leggete questo articolo, se siete al livello del mare,
state respirando ad una densità di 1,3 g/L (1,276 g/L
nei nostri calcoli). |
|
|
|
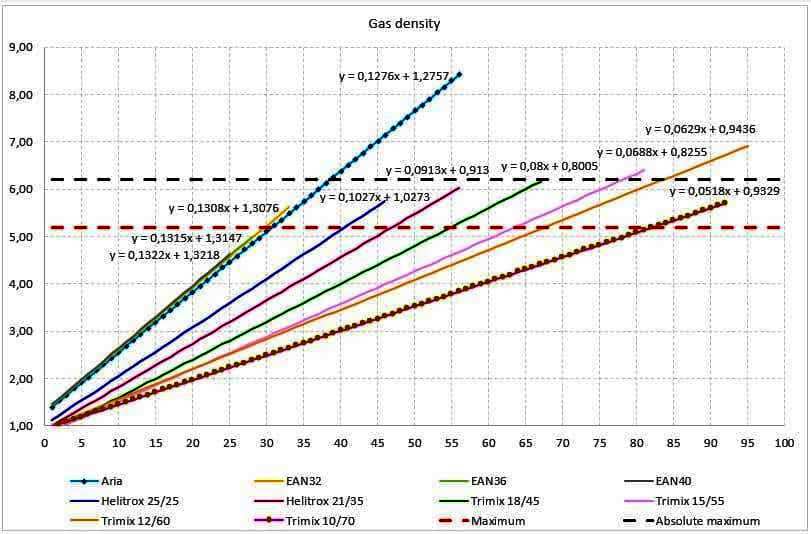
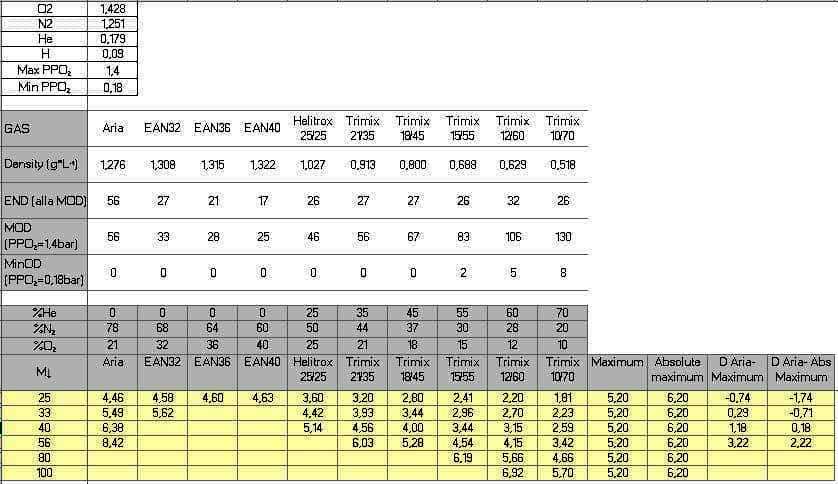
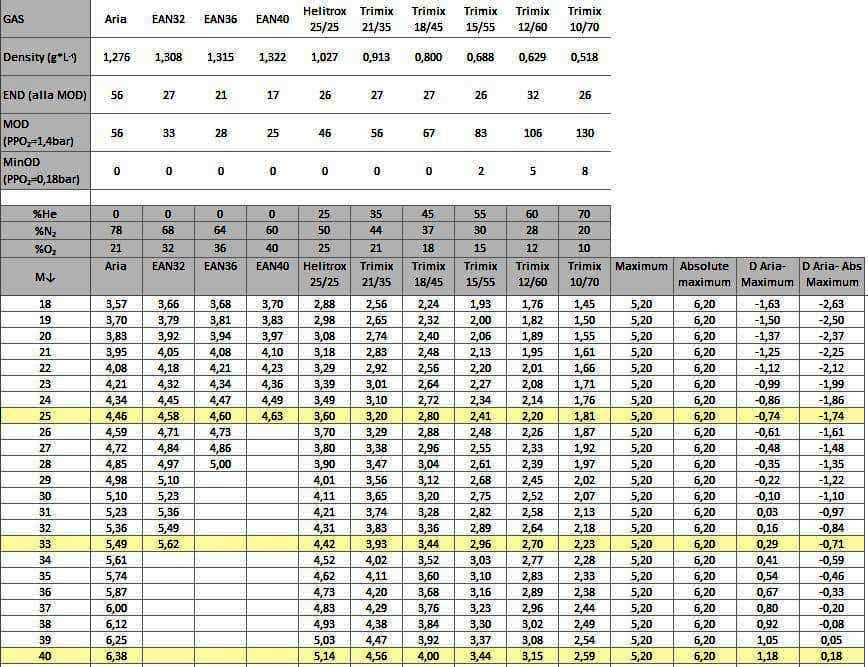
Per meglio comprendere le variazioni di densità dell’aria in base a temperatura ed umidità si rimanda all’articolo “La forma dell’aria” su "Teoria Subacquea". Proviamo a capire che danni provochi l’aumento della densità del gas in immersione. Il primo effetto è naturalmente l’incremento del WOB (Work Of Breathing), ossia il lavoro respiratorio, misurato in kPa. Per comprendere meglio la soglia di accettazione dello studio (8,5 kPa) basti pensare che se respirassimo da un tubo immersi in un metro d’acqua dovremmo vincere una resistenza simile (10 kPa), quindi uno sforzo non banale. Mentre la densità dei gas cresce secondo una relazione lineare data dall’applicazione della pressione alla loro densità al livello del mare, lo sforzo respiratorio varia a seconda degli individui (a parità di densità, non tutti hanno superato gli 8,5 kPa). Altro effetto del respirare miscele più dense è l’aumento della produzione della CO2 e la concomitante riduzione della capacità di eliminarla. Un processo che segue lo schema: + Densità >> + WOB >> + CO2 >> - smaltimento CO2 >> + CO2 La minore efficienza nello scambiare il Diossido di Carbonio è dovuta al non ottimale gradiente pressorio alveolare/arterioso. Analizziamo i numeri del lavoro Anthony/Mitchell osservando il grafico a barre dei successi/insuccessi a seconda della densità della miscela utilizzata: se la densità si attesta tra 6 e 7 g/L, la % di insuccesso per accumulo di CO2 è del 41%, a questa si somma un 12% per altre motivazioni (dispnea, stanchezza e problemi con l’attrezzatura). Il 53% dei subacquei non supera la prova con simili densità. Il tasso di fallimento scende al 20% con miscele tra i 5 e i 6 g/L. Una percentuale comunque elevata, ma nettamente inferiore a quella che ci si sarebbe aspettati se la correlazione fosse stata lineare. Vuol dire che se si supera una certa soglia di tolleranza, si arriva facilmente a superare valori critici di sforzo, ancor più pericolosi se si ricade nella categoria dei “ritentori di CO2”, ossia individui che non riescono a compensare l’incremento di Diossido di Carbonio con un aumento della frequenza respiratoria. A questo punto cerchiamo di calare l’evidenza teorica nella scelta delle miscele: iniziamo con il calcolare la densità di una miscela partendo dai valori dei singoli gas che la compongono. Iniziamo con il calcolare la densità di una miscela partendo dai valori dei singoli gas che la compongono. Le densità da considerare sono: Ossigeno: 1,428 g/L Azoto: 1,251 g/L Elio: 0,179 g/L L’aria è una miscela composta per il 78% da Azoto e il 21% da Ossigeno (per i nostri fini non consideriamo il restante 1% di gas vari). Per ottenerne la densità ponderiamo la densità dei singoli gas per il loro peso relativo. Da cui: Densità(Aria)=Densità(Azoto)*%(Azoto)+Densità(Ossigeno)*%(Ossigeno) In cifre: D(Aria)=1,251*0,78+1,428*0,21=1,276 g/L Generalizzando per le miscele ternarie (composte da tre gas): D(Miscela)=D(G1)*%(G1)+D(G2)*%(G2)+ D(G3)*%(G3) Applicando le formule appena citate si ricavano interessanti risultati per le miscele standard alle differenti profondità. Fissiamo la profondità e confrontiamo i risultati. A 25 metri si nota il leggero impatto dell’Ossigeno sulla densità complessiva. Il Nitrox (Ean32, 36, 40) mostra una densità leggermente superiore all’aria. Poco male, il vantaggio decompressivo (entro la MOD) compensa ampliamente il minimo sforzo respiratorio aggiuntivo. In sintesi, a 25 m avremo: Aria: 4,46 g/L EAN32: 4,58 g/L EAN36: 4,60 g/L EAN40: 4,63 g/L Nel grafico proposto potete vedere questi quattro gas praticamente sovrapposti. Nel medesimo grafico trovate anche l’equazione della retta che descrive la crescita lineare della densità al crescere della profondità e quindi della pressione assoluta. Ovvero: D=D(livello del mare)*Profondità. Il coefficiente angolare è esattamente la densità della miscela ad 1ATA. I lettori un po' più avvezzi alla matematica noteranno che per alcuni segmenti l’equazione non ha un coefficiente angolare coincidente con l’intercetta (provate a porre X=0, profondità=0). È dovuto al fatto che non vengono plottati valori inferiori alla profondità operativa minima per le miscele ipossiche, sotto il 18% di PPO2 non vengono considerate respirabili. |
|
|
|
Scendiamo un po' in profondità e chiamiamo in causa qualche miscela ternaria (Ossigeno, Elio, Azoto). Arriviamo a 33m, la MOD dell’EAN32 per una PPO2 massima di 1,4 ATA. (le approssimazioni le intendiamo in termini conservativi, per cui accettiamo 1,376 ATA dei 33 m e non 1,408 dei 34 m). Confrontiamo la densità di tre gas utilizzabili, due binari, Aria ed EAN32 ed uno ternario, Helitrox 25/25 (Ossigeno 25%, Elio 25%, Azoto 50%): Aria: 5,49 g/L EAN32: 5,62 g/L Helitrox 25/25: 4,42 g/L Per commentare quest’evidenza teniamo conto di quanto scrivono Anthony e Mitchell: “For the purposes of planning rebreather dives and in the current absence of more definitive or contradictory data, it seems prudent to recommend an ideal maximum gas density of 5.2 g·L-1 (equivalent to air diving at 31 m [102 ft]) and an absolute maximum of 6.2 g·L-1 (equivalent to air diving at 39 m [128 ft]).” Sono due i valori di riferimento: una soglia massima ideale di 5,2 g/L ed una assolutamente da non superare pari a 6,2 g/L (rispettivamente Maximum ed Absolute maximum nel grafico). Sui tre gas esaminati a 33 metri, ben due, sebbene di poco, superano la soglia massima ideale (Maximum). +0,29 g/L per l’aria e +0,42 g/L per l’EAN32. Facciamo lo stesso esercizio per una profondità di 40 metri, aggiungendo il Trimix 21/35 ed escludendo l’EAN32 per il superamento della MOD. Aria: 6,38 g/L Helitrox 25/25: 5,14 g/L Trimix 21/35: 4,56 g/L I
risultati interessanti sono due.
Spingiamoci ancora più giù fino alla MOD dell’aria (PPO2
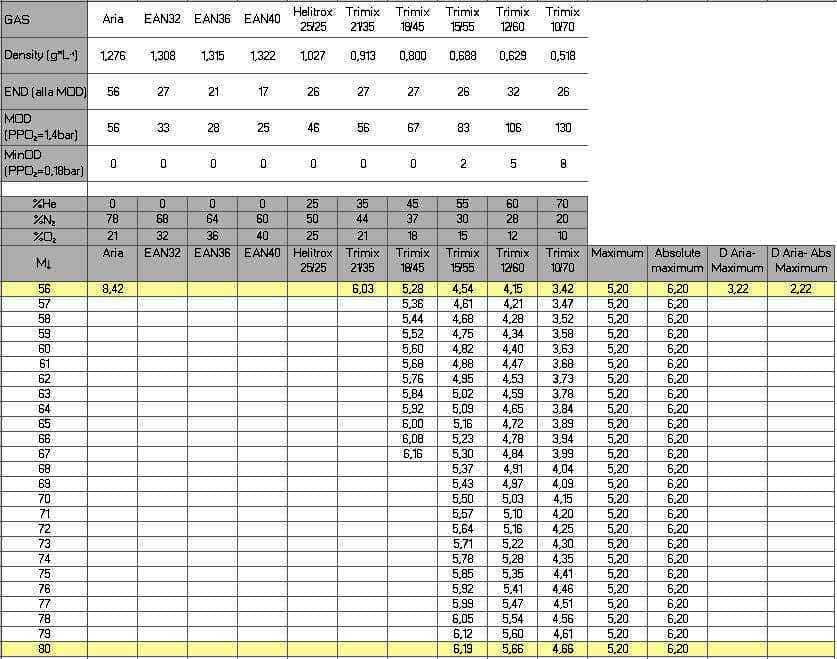
max=1,4 ATA), arriviamo a 56 metri. Aria: 8,42 g/L Trimix 21/35: 6,03 g/L Trimix 18/45: 5,28 g/L L’aria supera di 2,22 g/L l’Absolute maximum (6,2 g/L). Questo è uno dei tanti motivi per evitare le immersioni profonde con questa miscela. Ancora più in profondità consideriamo miscele ipossiche: Trimix 15/55, Trimix 12/60 e Trimix 10/70.
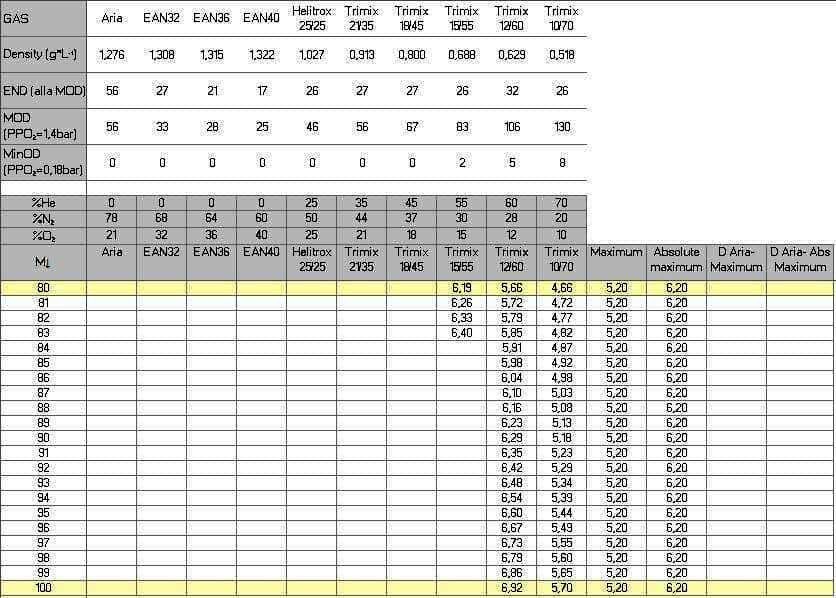
Ad 80 metri avremmo: Trimix 15/55: 6,19 g/L Trimix 12/60: 5,66 g/L Trimix 10/70: 4,66 g/L
A 100 metri avremmo: Trimix 12/60: 6,92 g/L Trimix 10/70: 5,70 g/L I gas sono quelli standard e vengono esaminati solo a titolo di esempio. A 100 m la PPO2 del 12/60 è pari ad 1,32 ATA, quindi determina un rapido accumulo di CNS% sul fondo, ciò è sconsigliabile come soluzione, se non per permanenze minime. A parte queste puntualizzazioni, ci preme sottolineare quanto cambi la densità della miscela anche per piccole frazioni di Elio aggiuntive. Il Trimix 10/70 a 100 m è ancora nel range di accettabilità di Anthony e Mitchell, mentre il 12/60 supera l’Absolute maximum. Nel grafico trovate riepilogate tutte le considerazioni appena esposte. Proponiamo anche gli screenshot del foglio elettronico utilizzato per le simulazioni. Per concludere: la densità delle miscele adottate dovrebbe essere una variabile da considerare nella pianificazione delle immersioni. ______________________________________________________________________________________________________________________ N.B. Quanto riportato è a puro titolo di esempio. Per la pianificazione delle immersioni e l’addestramento ci si deve rivolgere ad istruttori qualificati. |
|
|
|
|
|
|
|
|
|
Riferimenti Gavin Anthony1, Simon J. Mitchell2 * - Respiratory Physiology of Rebreather Diving - In: Pollock NW, Sellers SH, Godfrey JM, eds. Rebreathers and Scientific Diving. Proceedings of NPS/NOAA/DAN/AAUS June 16-19, 2015 Workshop. Durham, NC; 2016. 1 QinetiQ, Gosport, Hampshire, United Kingdom 2 Department of Anaesthesiology, University of Auckland, Auckland, New Zealand - sj.mitchell@auckland.ac.nz
(*)corresponding author
Vedi: https://m.facebook.com/story.php?story_fbid=140131864541995&id=110097917545390
|